
Aluminium, a właściwie glin, to najczęściej występujący pierwiastek (8%) w skorupie ziemskiej po tlenie (48%) i krzemie (28%). Należy do grupy tak zwanych metali nieżelaznych, bloku p układu okresowego. Aluminium jest także drugim po żelazie metalem pod względem zastosowań technicznych na świecie. Największymi rynkami zbytu aluminium są tradycyjnie sektor motoryzacyjny, budowlany, lotniczy oraz opakowaniowy. Jednak zanim trafia on w ręce producentów odpowiednich elementów, przechodzi długi i kosztowny proces produkcyjny.
Aluminium ma liczbę atomową równą 13, a jego masa atomowa wynosi 26,9815. Krystalizuje w sieci regularnej, ściennie centrowanej typu Al o parametrze 0,40408 nm. Temperatura topnienia aluminium wynosi 660°C, wrzenia 2494°C. Gęstość aluminium wynosi 2,6989 g/cm3 w temperaturze 20°C. Od symbolów Si (krzem) i Al powstała nazwa sial – najbardziej zewnętrzna warstwa skorupy ziemskiej tworząca kontynenty, w której znajdują się związki glinu. Aluminium jest zbyt reaktywne, by występować w naturze jako czysty metal. W połączeniu z innymi składnikami tworzy 270 znanych minerałów.
W 1808 roku Sir Humphrey Davy, brytyjski elektrochemik zaproponował nazwę aluminium jako techniczne określenie glinu, a siedemnaście lat później duński chemik Hans Christian Ørsted po raz pierwszy wyprodukował metaliczny glin (niektóre źródła wskazują na Friedricha Wöhlera w 1827 roku). W 1886 roku Amerykanin Charles Martin Hall i Francuz Paul Héroult, niezależnie od siebie opracowali metodę produkcji metalicznego glinu w procesie elektrolizy. Opatentowany proces Halla-Heroulta, gdzie tlenek glinu najpierw rozpuszczany jest w stopionym kriolicie, a następnie rozkładany elektrolitycznie na metaliczny glin oraz gazowy tlen pozostaje do dzisiaj główną przemysłową metodą wytwarzania czystego aluminium.
Rudy boksytu są podstawowym surowcem otrzymywania czystego Al2O3. Boksyt to ilasta skała osadowa składająca się głównie z wodorotlenków glinu (Al2O3× nH2O), wodorotlenków żelaza (Fe2O3 × nH2O), krzemionki oraz tlenku tytanu. Technologia pozyskiwania tlenku aluminium z rud boksytu została opracowana przez austriackiego chemika Karla Bayera w 1887 roku i w połączeniu z procesem Halla-Heroulta stanowi nierozłączną kompozycję produkcji aluminium pierwotnego. Obecnie aluminium wytwarza się w 17 gatunkach o różnym stopniu czystości od 99,99% do 99,00%.
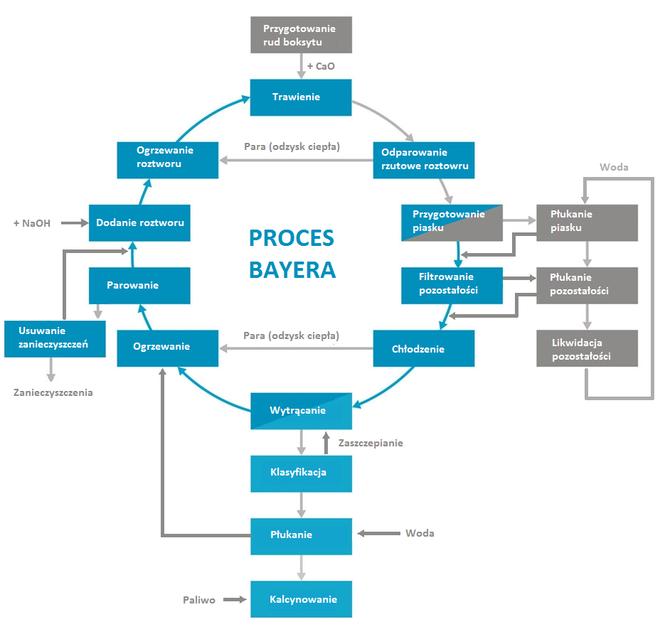
Tlenek glinu (Al2O3) wytwarzany jest z rud boksytu w procesie Bayera. Zakłady przetwórcze, do których trafia urobek w większości znajdują się w pobliżu kopalń. Proces produkcji tlenku aluminium można podzielić na trzy główne etapy: ekstrakcję, wytrącanie i kalcynację. Po wydobyciu ruda może zostać poddana zabiegowi przemywania wodą w celu usunięcia rozpuszczalnych zanieczyszczeń. Następnie surowiec uzupełnia się tlenkiem wapnia. Kompozycja jest kruszona w młynach rurowych do postaci ziaren o średnicy mniejszej niż 315 mikrometrów. Zwiększa to reaktywną powierzchnię właściwą cząstek, co wpływa na poprawę szybkości procesów ekstrakcji. Powstały proszek rozpuszcza się w gorącym, stężonym roztworze NaOH i przetrzymuje kilka godzin w komorach ciśnieniowych (autoklawach). Temperatura i ciśnienie są zależne od rodzaju boksytu i typu procesu. Podczas tego etapu zachodzą dwa zjawiska – rozpuszczanie tlenku glinu (dzięki amfoterycznemu charakterowi Al2O3) uwięzionego w boksycie oraz powstawanie osadów stałych nazywanych często „czerwonym szlamem”.
Krzemionka zawarta w boksycie reaguje z wodorotlenkiem sodu tworząc krzemian sodowy. W wyniku reakcji z rozpuszczonym glinianem sodowym powstaje nierozpuszczalny uwodniony glinokrzemian sodowy. Kontrola zawartości krzemionki w rudzie jest bardzo ważna, ze względu na straty Al2O3. Szlam powstaje z nierozpuszczalnych elementów w tym tlenku żelaza, który nadaje osadowi charakterystyczne, czerwone zabarwienie. W trakcie ekstrakcji następuje proces sedymentacji – oddzielenie cząstek stałych – szlamu od ługu zawierającego glinian sodowy w wyniku działania sił grawitacji. Kolejnym krokiem jest krystalizacja napędzana chłodzeniem roztworu. Powoduje ona rozkład roztworu na NaOH oraz Al(OH)3. Utworzone kryształy są klasyfikowane i rozdzielane według rozmiarów, tak jak na etapie filtracji tlenków. Zbyt małe są zawracane i wykorzystywane jako zarodki krystalizacji. Kryształy Al(OH)3 odpowiednich rozmiarów są przemywane wodą, a następnie suszone. Zużyty ług jest ogrzewany się i ponownie dopuszczony do obiegu.
Końcowym procesem jest kalcynacja wodorotlenku glinu, która przeprowadzana jest m.in. w lekko nachylonych piecach obrotowych w temperaturze 1000-1250°C. Prażenie powoduje usunięcie wilgoci, a czysty tlenek glinu w postaci białego proszku jest produktem końcowym w procesie Bayera, gotowym do wysyłki do pieców do wytopu metalicznego aluminium.
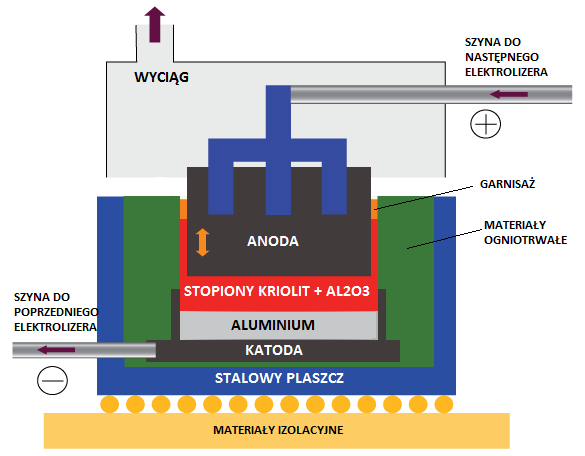
Następnym krokiem jest wytop aluminium w procesie elektrolizy Halla-Heroulta. Tlenek glinu jest rozkładany na metaliczny glin oraz gazowy tlen. Redukcję Al2O3 do metalicznego glinu przeprowadza się w stopionym roztworze kriolitu Na3AlF6 (około 75% masy elektrolitu) w średniej temperaturze 960°C. Przepływ prądu powoduje wydzielanie się na katodzie stopionego glinu o gęstości nieco wyższej od elektrolitu. Glin osadza się na dnie wanny. Na anodzie wyodrębnia się tlen, który reagując z grafitem daje mieszaninę CO oraz CO2. W celu podtrzymania zawartości tlenku glinu na poziomie 2 do 10% w roztopionej kąpieli (aby uniknąć przeskakiwania iskier z anody do katody) do wanien regularnie dodawany jest tlenek glinu. Powstające ciekłe aluminium jest oddzielane od elektrolitu oraz sukcesywnie usuwane z komory elektrolizera do tygli za pomocą syfonów próżniowych. Tygle transportowane są do urządzenia odlewniczego, a aluminium wprowadzane jest do pieców podgrzewających. W piecach tych dodawane są ewentualne dodatki stopowe.
Po etapie topienia aluminium następują procesy rafinacji ciekłego metalu. Rafinacja aluminium to zbiór procesów technologicznych mających na celu oczyszczenie metalu lub stopu z cząsteczek tlenków sodu, magnezu, wapnia, azotków, węglików, borków oraz wodoru gazowego. Końcowym stadium produkcji aluminium jest najczęściej odlewanie wlewków o cylindrycznej postaci, które po okresie homogenizacji wysyłane są do przedsiębiorstw produkujące aluminiowe elementy.
Źródło:
[1] Michalski B.: Rynek aluminium – Aluminium market. Wybrane międzynarodowe rynki towarowe, J. Rymarczyk, M. Niemiec (red.), Oficyna Wydawnicza Arboretum, Wrocław 2008, s. 263–287
[2] Farrokh M.: THERMODYNAMIC PROCESS MODELING AND SIMULATION OF A DIASPORE BAUXITE DIGESTION PROCESS, Mälardalen University Press Licentiate Theses No. 170 – 2013, s. 1-28
[3] http://electrochem.cwru.edu/encycl/art-a01-al-prod.htm [07.04.2014]
[4] http://www.d.umn.edu/~pmorton/geol2350/2007/powerpoints/chemistry.html [07.04.2014]
[5] http://scifun.chem.wisc.edu/chemweek/PDF/Aluminum.pdf [07.04.2014]
[6] http://www.chem.uwimona.edu.jm/lectures/bauxite.html [07.04.2014]
[7] http://alteo-alumina.com/en/bauxite-extraction [07.04.2014]
[8] http://gemini.net.pl/~marshall/technologia/alu/eliraf.htm [07.04.2014]
[9] http://bauxite.world-aluminium.org/refining/process.html [07.04.2014]
[10] “Aluminium” by Quinn Dombrowski, flickr.com CC BY-SA 2.0